Скачати цей тест
Всі тести у форматі PDF, презентації та Word документи для підготовки та викладання
Дізнатися більше
Укажіть із-поміж наведених назву процесу, під час якого середня кінетична енергія хаотичного руху молекул газу сталої маси зростає.
Г
ізобарне розширення
Правильна відповідь
Визначте, чи можна ідеальний газ певної кількості повернути в початковий стан у результаті послідовного перебігу процесів.
1. газ спочатку ізохорно нагрівають, потім ізобарно стискають, а наприкінці застосовують ізотермічний процес
2. газ спочатку ізохорно нагрівають, потім ізобарно збільшують його об’єм, а наприкінці застосовують ізотермічний процес
3. газ спочатку ізобарно стискають, потім ізохорно охолоджують, а наприкінці застосовують ізотермічний процес
4. спочатку ізобарно збільшують об'єм газу, потім газ ізохорно охолоджують, а наприкінці застосовують ізотермічний процес
Б
1, 3 – можна; 2, 4 – ні
Правильна відповідь
Двохатомний газ перебуває в камері під тиском $p_{0}$. Коли абсолютну температуру газу збільшили в 3 рази, відбулася повна дисоціація його молекул – усі вони розпалися на атоми. Яким став після цього тиск газу? Уважайте, що об'єм камери залишається сталим.
Г
$6 p_{0}$
Правильна відповідь
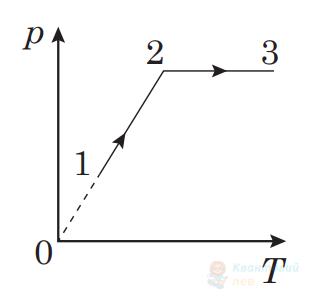
Ідеальний газ незмінної маси переходить зі стану 1 у стан 3 так, як відображає графік залежності тиску $p$ від абсолютної температури $T$. Визначте графік залежності тиску $p$ від об'єму $V$, який відповідає цьому переходу.
А
 Правильна відповідь
Правильна відповідь
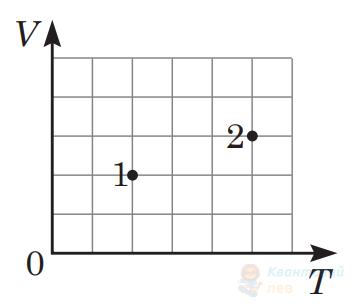
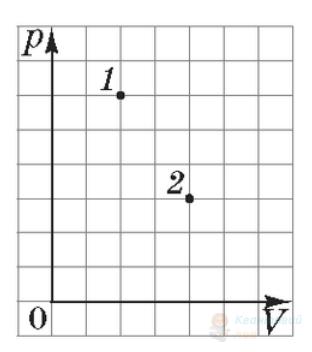
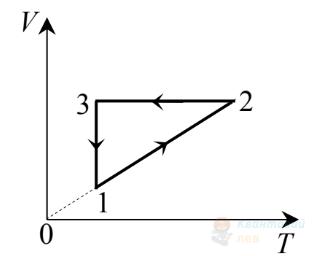
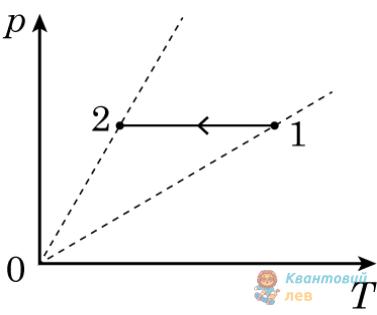
Укажіть рівність, яка встановлює правильне співвідношення між тисками $p_{1}$ та $p_{2}$ ідеального газу в станах 1 і 2 (див. рисунок) у системі координат $V T$, де $V$ – об'єм, $T$ – абсолютна температура. Маса газу стала.
А
$p_{2}=\frac{2}{5} p_{1}$
Б
$p_{2}=\frac{3}{2} p_{1}$
В
$p_{2}=\frac{5}{3} p_{1}$
Правильна відповідь
Г
$p_{2}=\frac{5}{2} p_{1}$
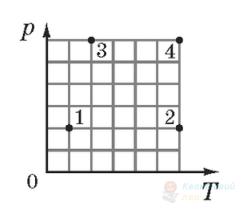
На кожному з чотирьох рисунків у координатах $V T$ (де $V$ – об'єм, $T$ – абсолютна температура) зображено точку (А – Г), координати якої відповідають параметрам стану ідеального газу кількістю речовини 1 моль. Яка точка відповідає стану газу з найбільшим тиском?
В
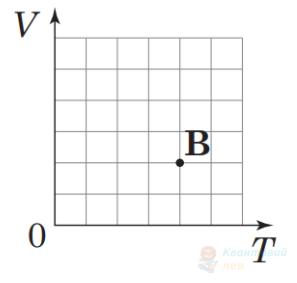 Правильна відповідь
Правильна відповідь
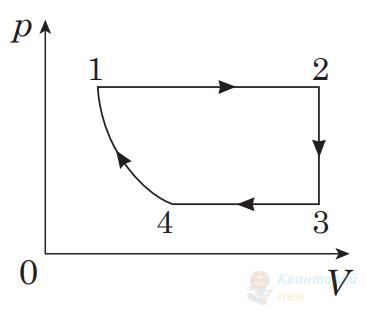
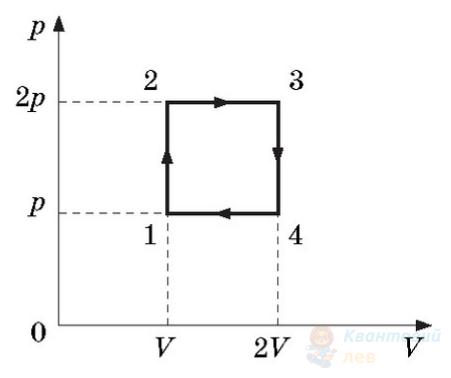
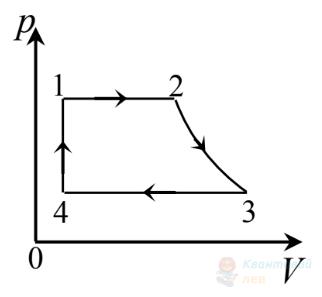
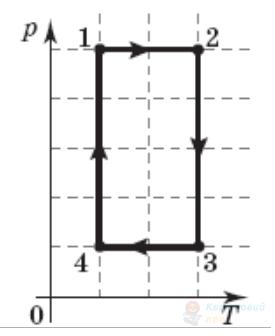
На рисунку в координатах $p V$ зображено замкнутий цикл 12341, здійснений газом незмінної маси (лінія 41 – частина гіперболи). Визначте вигляд цього циклу в координатах $p T$ ( $p$ – тиск, $T$ – температура, $V$ – об'єм).
А
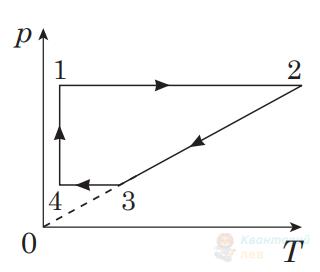 Правильна відповідь
Правильна відповідь
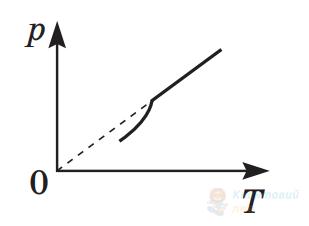
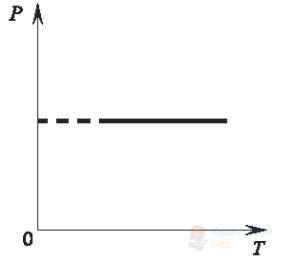
Під час досліду вивчають залежність тиску $p$ речовини від абсолютної температури $T$. Речовину в герметично закритій посудині, об'єм якої є незмінним, нагрівають. За наведеним графіком визначте початковий уміст посудини.
В
рідина та насичена пара
Правильна відповідь
Ідеальний газ незмінної маси переходить зі стану 1 у стан 3 так, як відображено на графіку залежності тиску $p$ від абсолютної температури $T$. Визначте роботу, яку виконав газ, якщо його початковий об'єм дорівнював $0,1 \mathrm{~м}^{3}$.
Г
$300 \mathrm{~Дж}$
Правильна відповідь
На графіку зображено цикл роботи теплової машини. На якій ділянці циклу температура підвищилася найбільше?
Вертикальна циліндрична посудина з гелієм (молярна маса гелію дорівнює $4 \mathrm{~г}/\mathrm{моль}$), що зверху закрита легкорухомим поршнем масою $4 \mathrm{~кг}$, знаходиться в повітрі, тиск якого становить $100 \mathrm{~кПа}$. Маса гелію дорівнює $16 \mathrm{~г}$, площа поперечного перерізу поршня становить $20 \mathrm{~см}^{2}$. Визначте, на скільки збільшиться об'єм, який займе газ, якщо його нагріти на $6 \mathrm{~К}$. Вважайте, що $g=10 \mathrm{~м} / \mathrm{с}^{2}$; універсальна газова стала дорівнює $8,3 \mathrm{~Дж} / ( \mathrm{моль} \cdot \mathrm{К} )$.
Г
$1660 \mathrm{~см}^{3}$
Правильна відповідь
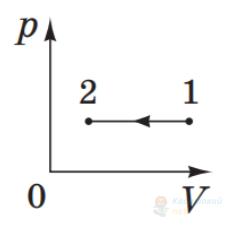
Над сталою масою газу здійснюється ізотермічний процес. Як змінився тиск газу, якщо об'єм зменшився у 9 разів?
В
збільшився у 9 разів
Правильна відповідь
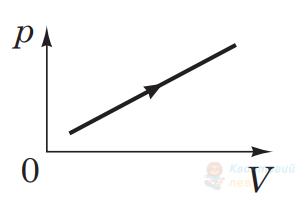
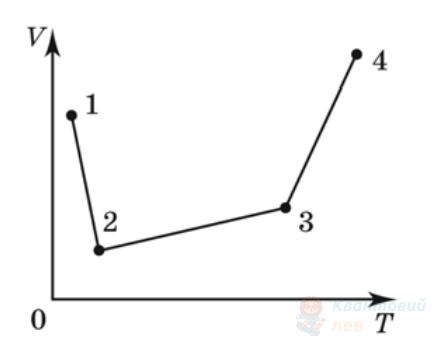
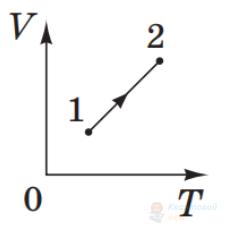
Визначте, як змінюються термодинамічні параметри (об'єм $V$, абсолютна температура $T$, тиск $p$ ) ідеального газу незмінної маси під час процесу, графік якого наведено на рисунку.
А
$V, T, p$ збільшуються
Правильна відповідь
Б
$V, p$ збільшуються, $T$ не змінюється
В
$T, p$ збільшуються, $V$ зменшується
Г
$V, p$ збільшуються, $T$ зменшується
Точки на рисунку відповідають різним станам однієї й тієї самої маси ідеального газу ( $p$ – тиск, $T$ – температура). У якому стані об'єм газу найбільший?
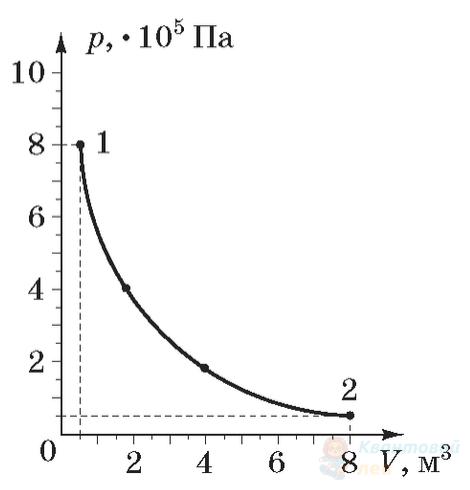
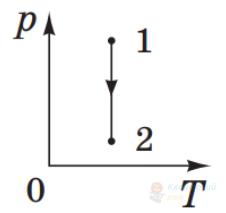
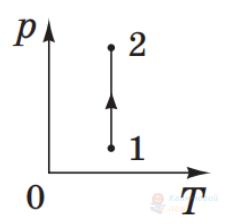
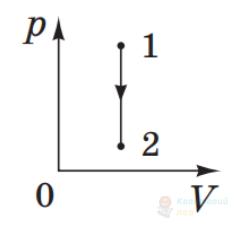
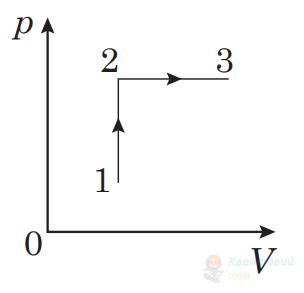
Який процес дозволяє перевести ідеальний газ певної маси зі стану 1 у стан 2 (див. рисунок у системі координат $pV$, де $p$ – тиск, $V$ – об'єм)?
А
ізотермічний
Правильна відповідь
Під час якого з газових процесів концентрація молекул газу не може змінитися?
А
людина набирає повітря в легені
Б
повітря виходить із пробитої шини
В
насичену водяну пару охолоджують
Г
кисень у закритому балоні остигає, коли вимикають опалення
Правильна відповідь
У посудині, закритій рухомим поршнем, знаходиться ідеальний газ. На рисунку зображено залежність об'єму газу від абсолютної температури. У якому стані тиск газу найбільший?
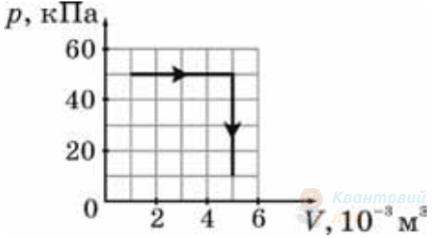
Ідеальний газ під поршнем у закритій посудині переходить зі стану 1 у стан 2 так, як зображено на графіку, де $p$ – тиск, $V$ – об'єм. Унаслідок цього газ отримав від навколишнього середовища $3 \cdot 10^{5} \mathrm{~Дж}$ енергії. Яку роботу над газом виконують зовнішні сили?
А
$-300 \mathrm{~кДж}$
Правильна відповідь
На рисунку в координатах $p, V$ зображений замкнутий цикл 12341, здійснений незмінною масою газу (лінія 23 – частина гіперболи). Визначте, який вигляд має даний цикл у координатах $p, T$.
В
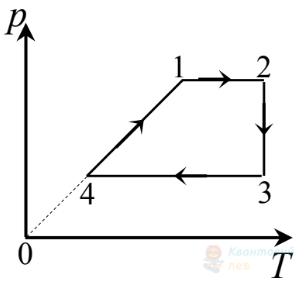 Правильна відповідь
Правильна відповідь
Початковий об'єм газу становить $60 \mathrm{~л}$. Визначте, яким стане об'єм цієї маси газу, якщо абсолютна температура підвищиться від $300 \mathrm{~К}$ до $450 \mathrm{~К}$, а тиск зменшиться в 2 рази.
Г
$180 \mathrm{~л}$
Правильна відповідь
На рисунку в системі координат $V, T$ зображено замкнутий цикл 1231, здійснений газом сталої маси. Визначте, який вигляд має графік цього циклу в системі координат $p, V$.
В
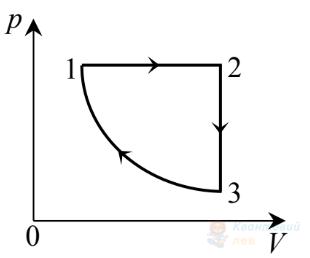 Правильна відповідь
Правильна відповідь
Визначте, якою буде абсолютна температура певної маси ідеального газу, якщо тиск газу збільшити на $25 \%$, а об'єм зменшити на $20 \%$. Початкова температура газу дорівнює $300 \mathrm{~К}$.
Б
$300 \mathrm{~К}$
Правильна відповідь
Визначте, яку роботу виконує розріджений азот масою $56 \mathrm{~г}$ під час ізобарного нагрівання на $50 \mathrm{~К}$. Молярна маса азоту дорівнює $28 \mathrm{~г}/\mathrm{моль}$, а універсальна газова стала $8,3 \mathrm{~Дж} / ( \mathrm{моль} \cdot \mathrm{К} )$.
В
$830 \mathrm{~Дж}$
Правильна відповідь
У балоні знаходилося $0,3 \mathrm{~кг}$ гелію. Через деякий час у результаті витоку гелію та зменшення абсолютної температури на $10 \%$ тиск у балоні зменшився на $20 \%$. Визначте, скільки молекул гелію просочилося з балона. $N_{\mathrm{A}} = 6 \cdot 10^{-23} \mathrm{~моль}^{-1}$; молярна маса гелію дорівнює $4 \cdot 10^{-3} \mathrm{~кг} / \mathrm{моль}$.
В
$5 \cdot 10^{24}$
Правильна відповідь
Визначте, який із зазначених процесів з ідеальним газом міг бути ізотермічним.
А
тиск і об'єм газу збільшилися вдвічі
Б
тиск газу зменшився вдвічі, а об'єм збільшився вдвічі
Правильна відповідь
В
тиск газу зменшився вдвічі, а об'єм збільшився в 4 рази
Г
тиск і об'єм газу зменшилися вдвічі
У балоні знаходилося $0,3 \mathrm{~кг}$ гелію. Через деякий час у результаті витоку гелію та зменшення абсолютної температури на $10\ \%$ тиск у балоні зменшився. Визначте, на скільки відсотків зменшився тиск у балоні, якщо відомо, що назовні з балона просочилося $5 \cdot 10^{24}$ молекул. $N_{\mathrm{A}} = 6 \cdot 10^{-23} \mathrm{~моль}^{-1}$; молярна маса гелію дорівнює $4 \cdot 10^{-3} \mathrm{~кг} / \mathrm{моль}$.
Б
$20\ \%$
Правильна відповідь
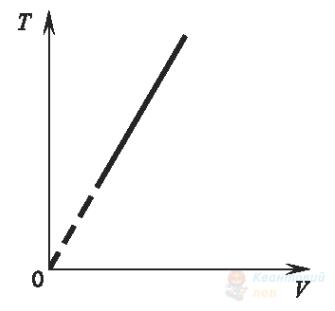
На рисунку зображено графік залежності абсолютної температури ідеального газу від його об’єму. Виберіть рисунок, на якому зображено графік цього процесу в системі інших термодинамічних координат.
В
 Правильна відповідь
Правильна відповідь
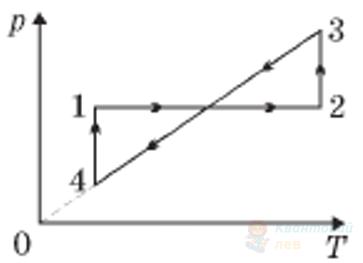
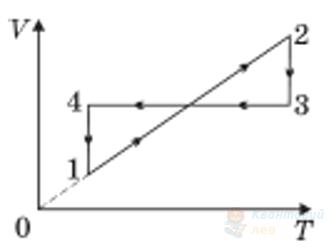
На рисунку в системі координат $p, T$ зображено замкнутий цикл 12341, здійснений газом сталої маси. Установіть, який вигляд має графік цього циклу в системі координат $V, T$.
А
 Правильна відповідь
Правильна відповідь
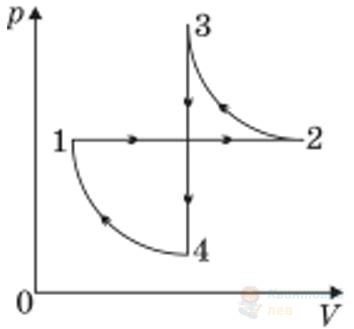
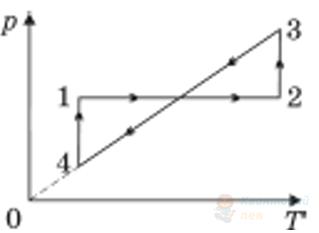
На рисунку в системі координат $p, V$ зображено замкнутий цикл 12341, здійснений газом сталої маси (лінії 23 та 41 – частини гіперболі. Установіть, який вигляд має графік цього циклу в системі координат $p, T$.
В
 Правильна відповідь
Правильна відповідь
На рисунку зображено графік залежності тиску $\large p$ ідеального газу сталої маси від абсолютної температури $T$.
Як змінились об'єм газу й середня квадратична швидкість руху його молекул під час переходу зі стану 1 у стан 2?
Б
зменшився; зменшилася
Правильна відповідь
Установіть відповідність між назвами формул (1-4), що стосуються молекулярно-кінетичної теорії та термодинаміки, та самими формулами (А – Д).
Позначення: $p$ – тиск ідеального газу, $n$ – концентрація молекул газу, $m_{0}$ – маса молекули, $m$ – маса газу, $M$ – молярна маса, $\bar{v}$ – середня швидкість молекули, $k$ – стала Больцмана, $R$ – універсальна газова стала, $T$ – температура, $U$ – внутрішня енергія, $Q$ – кількість теплоти, $A$ – робота, $c$ – питома теплоємність.
Варіанти зліва
1
основне рівняння молекулярно-кінетичної теорії ідеального газу
2
перший закон термодинаміки
3
загальне рівняння стану ідеального газу для довільної його кількості
4
середня кінетична енергія молекул одноатомного газу
Варіанти справа
А
$p=\frac{1}{3} n m_{0} \bar{v}^{2}$
Б
$\bar{E}=\frac{3}{2} k T$
Установіть відповідність між назвою ізопроцесу, що відбувається з ідеальним газом сталої маси, і графіком, який відповідає цьому процесу ( $p$ – тиск, $V$ – об'єм, $T$ – температура).
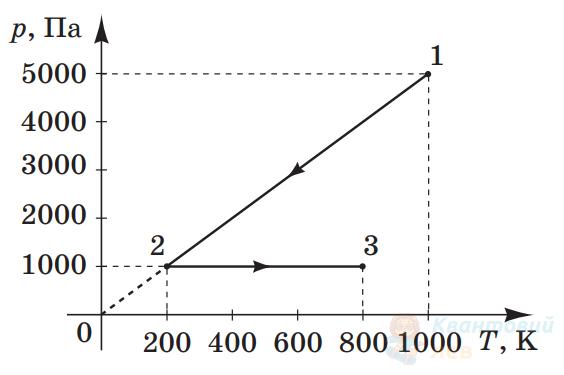
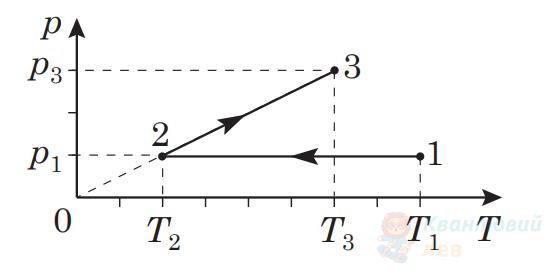
На рисунку зображено графік зміни стану ідеального газу в координатах $p T$, де $p-$ тиск, $T$ – абсолютна температура. Маса газу – стала.
Визначте, яку роботу виконав газ під час переходу зі стану 2 в стан 3.
Відповідь запишіть у джоулях ($\mathrm{Дж}$).
Балон об'ємом $0,83 \mathrm{~м}^{3}$ за температури $250 \mathrm{~К}$ під тиском $100 \mathrm{~кПа}$ заповнено киснем. Після того як у балон додали ще кисню, тиск газу збільшився до $195 \mathrm{~кПа}$, а його температура – до $300 \mathrm{~К}$. Уважайте, що молярна маса кисню $32 \mathrm{~г}/\mathrm{моль}$, а універсальна газова стала дорівнює $8,3 \mathrm{~Дж}/(\mathrm{моль} \cdot \mathrm{К})$.
Обчисліть кількість речовини в балоні перед додаванням кисню.
Відповідь запишіть у молях ($\mathrm{моль}$).
Правильна відповідь:
40.0
Балон об'ємом $0,83 \mathrm{~м}^{3}$ за температури $250 \mathrm{~К}$ під тиском $100 \mathrm{~кПа}$ заповнено киснем. Після того як у балон додали ще кисню, тиск газу збільшився до $195 \mathrm{~кПа}$, а його температура – до $300 \mathrm{~К}$. Уважайте, що молярна маса кисню $32 \mathrm{~г}/\mathrm{моль}$, а універсальна газова стала дорівнює $8,3 \mathrm{~Дж}/(\mathrm{моль} \cdot \mathrm{К})$.
Обчисліть масу кисню, який додали в балон.
Відповідь запишіть у кілограмах ($\mathrm{кг}$).
Унаслідок ізотермічного стискання ідеального газу від об'єму $8 \mathrm{~л}$ до об'єму $6 \mathrm{~л}$ його тиск збільшився на $4 \mathrm{~кПа}$. Визначте початковий тиск газу.
Відповідь запишіть у кілопаскалях ($\mathrm{кПа}$).
Правильна відповідь:
12.0
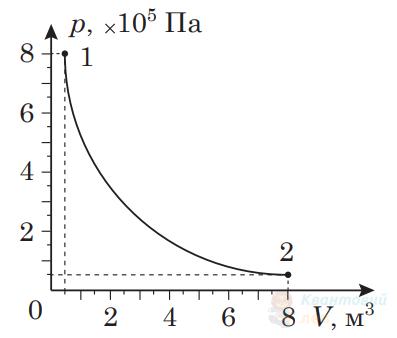
Ідеальний газ під поршнем у закритій посудині перейшов зі стану 1 у стан 2 так, як зображено на графіку, який є частиною гіперболи, де $p$ – тиск, $V$ – об'єм. Унаслідок цього газ отримав від навколишнього середовища кількість теплоти $3 \cdot 10^{5} \mathrm{~Дж}$.
Визначте кінцевий тиск (стан 2) ідеального газу.
Відповідь запишіть у кілопаскалях ($\mathrm{кПа}$)
Правильна відповідь:
50.0
Під час ізобарного нагрівання ідеальний одноатомний газ сталої маси виконав роботу $8 \mathrm{~кДж}$. Яку кількість теплоти надано газу?
Відповідь запишіть у кілоджоулях ($\mathrm{кДж}$).
Правильна відповідь:
20.0
Футбольний м’яч сферичної форми має сталий об'єм $5,5 \mathrm{~л}$. Початковий тиск у м’ячі дорівнює атмосферному й становить $100 \mathrm{~кПа}$. Його накачують за допомогою насоса, робочий об'єм якого дорівнює $0,1 \mathrm{~л}$. Визначте тиск повітря в м'ячі після 11 циклів роботи насоса. Стискання повітря відбувається за сталої температури.
Відповідь запишіть у кілопаскалях ($\mathrm{кПа}$).
Правильна відповідь:
120.0
В експерименті для охолодження зразків використовували зріджений гелій об’ємом $4 \mathrm{~л}$. Половина гелію випарувалася. Його було зібрано та перекачано до резервуару сталого об’єму $24,9 \mathrm{~м}^{3}$, у якому вже був гелій за температури $300 \mathrm{~К}$ і тиску $10^{5} \mathrm{~Па}$. Температура в резервуарі не змінюється. Уважайте, що молярна маса гелію становить $4 \mathrm{~г}/\mathrm{моль}$, густина зрідженого гелію – $0,125 \mathrm{~г} / \mathrm{см}^{3}$, універсальна газова стала дорівнює $8,3 \mathrm{~Дж} / ( \mathrm{моль} \cdot \mathrm{К} )$ .
Яка кількість речовини ($\mathrm{моль}$) виявилася в резервуарі після експерименту?
Правильна відповідь:
1062.5
В автомобільному газовому балоні із метаном $\left(\mathrm{CH}_{4}\right)$ місткістю $83 \mathrm{~л}$ тиск дорівнює $150 \mathrm{~атм}$ , температура становить $27^{\circ} \mathrm{C}$. Визначте кількість теплоти, що виділиться внаслідок згоряння всього метану, якщо питома теплота його згоряння $50 \mathrm{~МДж} / \mathrm{кг}$. Уважайте, що універсальна газова стала дорівнює $8,3 \mathrm{~Дж} / ( \mathrm{моль} \cdot \mathrm{К} )$, а одна атмосфера становить $10^{5} \mathrm{~Па}$. Молярна маса метану $\left(\mathrm{CH}_{4}\right)$ дорівнює $16 \mathrm{~г}/\mathrm{моль}$. Відповідь запишіть у мегаджоулях.
Правильна відповідь:
400.0
В експерименті для охолодження зразків використовували зріджений гелій об’ємом $4 \mathrm{~л}$. Половина гелію випарувалася. Його було зібрано та перекачано до резервуару сталого об’єму $24,9 \mathrm{~м}^{3}$, у якому вже був гелій за температури $300 \mathrm{~К}$ і тиску $10^{5} \mathrm{~Па}$. Температура в резервуарі не змінюється. Уважайте, що молярна маса гелію становить $4 \mathrm{~г}/\mathrm{моль}$, густина зрідженого гелію – $0,125 \mathrm{~г} / \mathrm{см}^{3}$, універсальна газова стала дорівнює $8,3 \mathrm{~Дж} / ( \mathrm{моль} \cdot \mathrm{К} )$ .
На скільки відсотків збільшився тиск гелію в резервуарі?
Правильна відповідь:
6.25
У посудину об'ємом $0,83 \mathrm{~м}^{3}$ налили воду. Потім посудину герметично закрили та нагріли воду до температури $100^{\circ} \mathrm{C}$. Уся вода випарувалася й створила тиск $10^{5} \mathrm{~Па}$. Уважайте, що молярна маса води дорівнює $18 \cdot 10^{-3} \mathrm{~кг}/\mathrm{моль}$, універсальна газова стала становить $8,3 \mathrm{~Дж} / ( \mathrm{моль} \cdot \mathrm{К} )$.
Визначте масу води, яку налили в посудину.
Відповідь запишіть у кілограмах ($\mathrm{кг}$) і округліть до сотих.
Правильна відповідь:
0.48
Визначте кількість речовини газу, якщо за температури $7^{\circ} \mathrm{C}$ і тиску $166 \mathrm{~кПа}$ об'єм газу дорівнює $70 \mathrm{~л}$. Уважайте, що універсальна газова стала дорівнює $8,3 \mathrm{~Дж}/(\mathrm{моль} \cdot \mathrm{К})$.
Відповідь запишіть у молях
На рисунку в системі координат $p, T$ зображено замкнутий цикл 12341 теплової машини, у якої робочим тілом є ідеальний газ. Визначте співвідношення $\frac{A_{1-2}}{A_{3-4}}$ абсолютних значень робіт газу на ділянках $1-2$ і $3-4$.
Циліндрична закрита посудина висотою $1,2 \mathrm{~м}$ знаходиться у вертикальному положенні і розділена на дві частини невагомим тонким поршнем, що ковзає без тертя. На якій висоті установиться поршень, якщо у верхній частині посудини знаходиться гелій, молярна маса якого дорівнює $0,004 \mathrm{~кг}/\mathrm{моль}$, а у нижній – азот, молярна маса якого $0,028 \mathrm{~кг}/\mathrm{моль}$. Температури і маси газів в обох частинах посудини однакові. Відповідь запишіть у метрах.
Правильна відповідь:
0.15
Футбольний м'яч об'ємом $3 \mathrm{~л}$ накачують поршневим насосом до тиску $2 \cdot 10^{5} \mathrm{~Па}$. Скільки накачувань потрібно зробити, якщо за кожне накачування до м'яча надходить повітря об'ємом $300 \mathrm{~см}^{3}$ ? Уважайте, що атмосферний тиск становить $1 \cdot 10^{5} \mathrm{~Па}$.
Правильна відповідь:
10.0
Кисень знаходиться в балоні під тиском $2,075 \cdot 10^{5} \mathrm{~Па}$. Температура в балоні дорівнює $47^{\circ} \mathrm{C}$. Яку густину має кисень? Молярна маса кисню становить $0,032 \mathrm{~кг}/\mathrm{моль}$; універсальна газова стала дорівнює $8,3 \mathrm{~Дж} / ( \mathrm{моль} \cdot \mathrm{К} )$. Відповідь запишіть у $\mathrm{кг} / \mathrm{м}^{3}$.
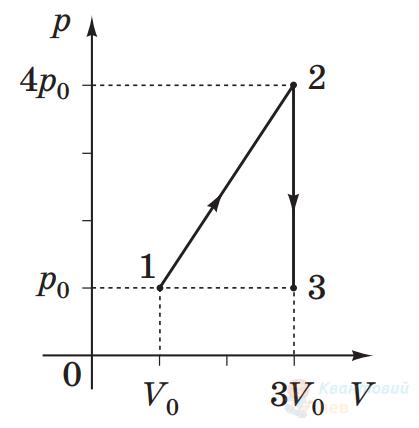
З ідеальним одноатомним газом незмінної маси відбуваються процеси $1-2-3$, що відображені на графіку (див. рисунок). Яку кількість теплоти отримав газ у процесах $1-2-3$, якщо $p_{0}=1 \cdot 10^{5} \mathrm{~Па}$, $V_{0}=2 \mathrm{~л}$?
Відповідь запишіть у кілоджоулях.
Ідеальний одноатомний газ знаходиться в посудині з твердими стінками об'ємом $0,5 \mathrm{~м}^{3}$. Унаслідок нагрівання його тиск збільшився на $6 \cdot 10^{3} \mathrm{~Па}$. На скільки збільшилася внутрішня енергія газу? Відповідь запишіть у кілоджоулях.
Для різання металу з газового балона місткістю $83 \mathrm{~л}$ і робочим тиском 70 атм використано кисень масою $2 \mathrm{~кг}$. Яка маса ($\mathrm{кг}$) кисню, що залишився в балоні? Температура газу в балоні становить $7^{\circ} \mathrm{C}$. Уважайте, що універсальна газова стала дорівнює $8,3 \mathrm{~Дж} / ( \mathrm{моль} \cdot \mathrm{К} )$, молярна маса кисню – $0,032 \mathrm{~кг}/\mathrm{моль}$, 1 атм $=10^{5} \mathrm{~Па}$.
Повітряна куля з газонепроникною оболонкою масою $400 \mathrm{~кг}$ заповнена гелієм. Куля може нерухомо утримувати вантаж масою $225 \mathrm{~кг}$ у повітрі на певній висоті. Визначте масу гелію в кулі. Вважайте, що об'єм вантажу малий, а оболонка кулі не спричиняє опору зміні об'єму кулі і є тонкою. Молярна маса гелію дорівнює $4 \cdot 10^{-3} \mathrm{~кг} / \mathrm{моль}$. Повітря вважайте газом з молярною масою $29 \cdot 10^{-3} \mathrm{~кг} / \mathrm{моль}$. Гелій і повітря вважайте ідеальними газами. Відповідь запишіть у кілограмах.
Правильна відповідь:
100.0
З балона випустили $2 \mathrm{~г}$ газу, в результаті чого тиск у ньому знизився на $10\ \%$. Визначте (у $\mathrm{м}^{3}$) місткість балона, якщо густина газу в початковий момент була $0,2 \mathrm{~кг} / \mathrm{м}^{3}$. Температура газу в балоні не змінювалася.
Визначте кількість теплоти, яку отримав ідеальний газ під час процесу, зображеного на графіку. Урахуйте, що внутрішня енергія ідеального газу залежить тільки від його температури.
Відповідь запишіть у джоулях.
Правильна відповідь:
200.0
Визначте густину водню за температури $27^{\circ}\mathrm{C}$ й тиску $2,49 \cdot 10^{5} \mathrm{~Па}$. Молярна маса водню становить $2 \cdot 10^{-3} \mathrm{~кг} / \mathrm{моль}$.
Універсальна газова стала дорівнює $8,3 \mathrm{~Дж} / ( \mathrm{моль} \cdot \mathrm{К} )$. Уважайте водень за цих умов ідеальним газом.
Відповідь запишіть у кілограмах на метр кубічний ($\mathrm{кг} / \mathrm{м}^3$).